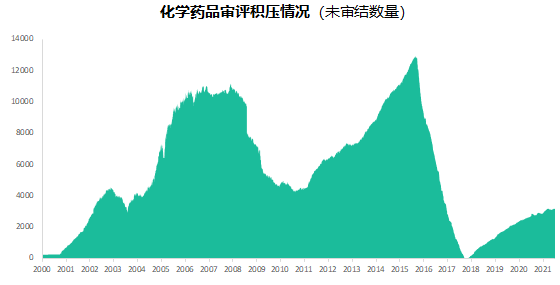
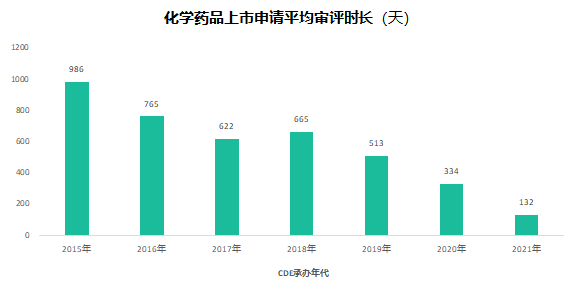
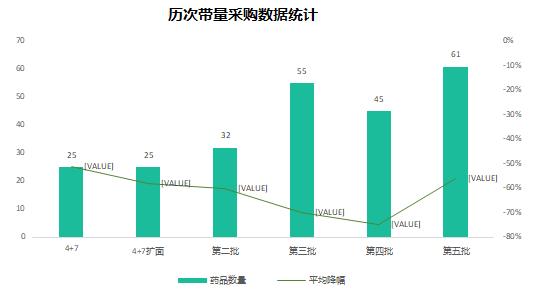
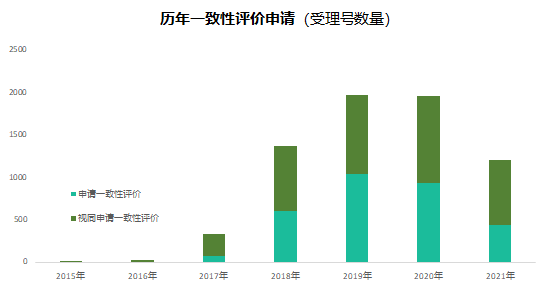
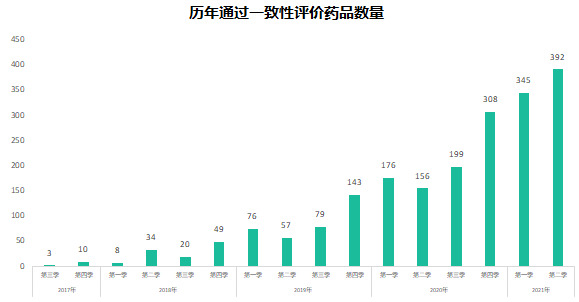
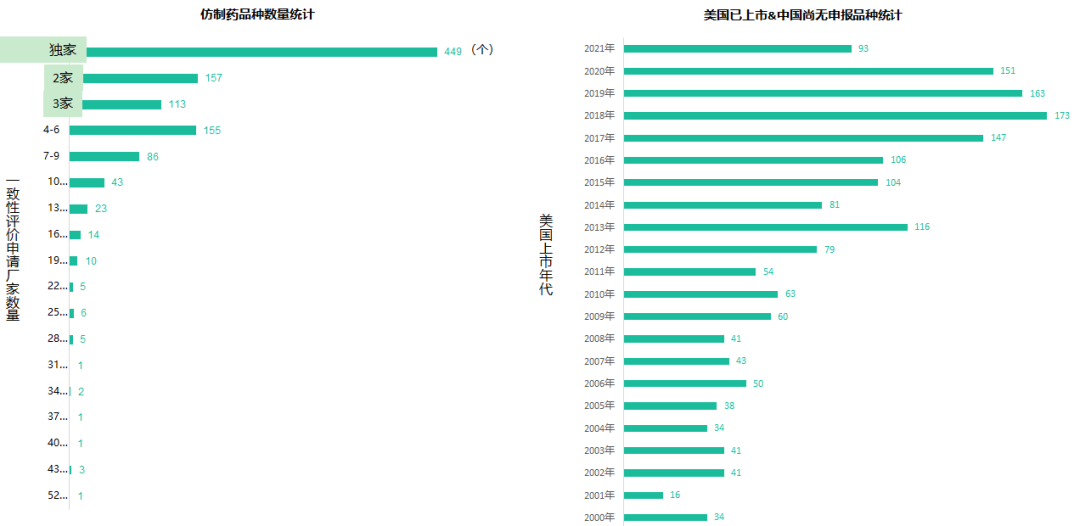
六年前的7月22日,國家食品藥品監(jiān)督管理總局發(fā)布《關(guān)于開展藥物臨床試驗(yàn)數(shù)據(jù)自查核查工作的公告》(2015年第117號(hào)),正式拉開藥品監(jiān)管制度深化改革的序幕�。隨后�,《關(guān)于深化審評(píng)審批制度改革鼓勵(lì)藥品醫(yī)療器械創(chuàng)新的意見》發(fā)布,明確了藥品醫(yī)療器械審評(píng)審批改革的目標(biāo)����、任務(wù)和具體措施,也宣告解決藥品審評(píng)積壓�����、提高藥品審批質(zhì)量和仿制藥水平的工作強(qiáng)力開啟��。6年時(shí)光����,轉(zhuǎn)瞬即逝�����,有歡樂�����、有痛苦�、有迷茫也有堅(jiān)定;6年間����,中國的仿制藥開發(fā)都有哪些變化�����,不妨隨我們一起回顧���。審評(píng)審批制度改革意見共提出了5大目標(biāo)和12項(xiàng)措施,其中�,提高審評(píng)審批質(zhì)量和解決注冊(cè)申請(qǐng)積壓正是5大目標(biāo)之一,目的是要建立科學(xué)���、高效的審評(píng)審批體系和按規(guī)定時(shí)限完成藥品審批�。醫(yī)藥魔方PharmaGo數(shù)據(jù)顯示��,CDE在2017年底就解決了申請(qǐng)積壓的問題�。此后,CDE又逐步實(shí)施增加審評(píng)隊(duì)伍�����、提高審評(píng)質(zhì)量����、提高仿制藥質(zhì)量標(biāo)準(zhǔn)�����、推進(jìn)一致性評(píng)價(jià)等舉措��,從人力和制度上進(jìn)一步解決造成審批積壓的原因�。與此同時(shí)���,可以看到CDE的審評(píng)審批速度實(shí)現(xiàn)了大幅提升。對(duì)于新申報(bào)的化學(xué)藥品上市申請(qǐng)�,已經(jīng)由2015年的986天提高至2020年的334天。2020年7月新版《藥品注冊(cè)管理辦法》開始執(zhí)行���,明確要求化學(xué)藥品上市申請(qǐng)審批期限為200日�����,這一目標(biāo)已經(jīng)在2021年申報(bào)的藥品審評(píng)中有所體現(xiàn)����。存量仿制藥一致性評(píng)價(jià)逐漸退出2018年底���,國家藥品監(jiān)督管理局發(fā)布的《關(guān)于仿制藥質(zhì)量和療效一致性評(píng)價(jià)有關(guān)事項(xiàng)的公告》指出�����,對(duì)通過仿制藥質(zhì)量和療效一致性評(píng)價(jià)的品種優(yōu)先納入目錄���,未通過一致性評(píng)價(jià)的品種將逐步被調(diào)出目錄����,并充分考慮基本藥物保障臨床需求的重要性�,對(duì)納入國家基本藥物目錄的品種,不再統(tǒng)一設(shè)置基本藥物評(píng)價(jià)時(shí)限要求��。此舉說明國家藥品監(jiān)督管理局不再統(tǒng)一要求在2018年底前完成基本藥物的一致性評(píng)價(jià)�。不過,仿制藥一致性評(píng)價(jià)已經(jīng)成為企業(yè)的常態(tài)化行為���,尤其在國家執(zhí)行的帶量采購中����,未通過仿制藥一致性評(píng)價(jià)就沒有申報(bào)資格�����。同時(shí)�����,帶量采購也趨于合理化,不會(huì)刻意壓縮企業(yè)的合理利潤(rùn)��。在剛結(jié)束的第五批帶量采購中����,不僅藥品中標(biāo)數(shù)量歷年最多,藥品價(jià)格也首次出現(xiàn)相對(duì)上漲���。龐大的市場(chǎng)銷量�,成為推動(dòng)企業(yè)加速完成仿制藥一致性評(píng)價(jià)的動(dòng)力�����。根據(jù)PharmaGo的數(shù)據(jù)�,2019年成為仿制藥申請(qǐng)一致性評(píng)價(jià)的頂峰�。隨著2020年7月新版《藥品注冊(cè)管理辦法》正式執(zhí)行,按新注冊(cè)分類申報(bào)的仿制藥視同通過一致性評(píng)價(jià)�����,存量仿制藥申請(qǐng)一致性評(píng)價(jià)的數(shù)量逐漸走低��。與之相對(duì)應(yīng),獲批通過仿制藥一致性評(píng)價(jià)的產(chǎn)品數(shù)量也在不斷增加�。預(yù)示著,企業(yè)正在加速完成仿制藥的一致性評(píng)價(jià)工作��。隨著企業(yè)完成自己的戰(zhàn)略品種的一致性評(píng)價(jià)���,存量仿制藥的一致性評(píng)價(jià)也必將被新注冊(cè)分類申報(bào)所替代���。以上是基于藥品注冊(cè)歷史數(shù)據(jù)對(duì)過去6年我國仿制藥開發(fā)變化的一個(gè)概覽,以及對(duì)未來仿制藥注冊(cè)申報(bào)趨勢(shì)的一個(gè)推演����。如果從品種競(jìng)爭(zhēng)的角度去看,中國仿制藥開發(fā)一直存在兩種極端現(xiàn)象��,一方面是同質(zhì)化競(jìng)爭(zhēng)��,重復(fù)嚴(yán)重���。即便總局發(fā)布多批過度重復(fù)藥品目錄對(duì)行業(yè)進(jìn)行引導(dǎo)和警示�,藥企扎堆申報(bào)熱門品種的現(xiàn)象仍然存在���。尤其他達(dá)拉非�����,2005年至今一直是企業(yè)熱衷的藥物品種�;此外,阿哌沙班�����、利伐沙班等藥物的申報(bào)熱度也始終未見衰退���。另一方面���,與過度重復(fù)申報(bào)截然相反,中國仿制藥的獨(dú)家品種仍然占據(jù)過高的比例����,目前有449個(gè)品種僅一家企業(yè)申報(bào)一致性評(píng)價(jià)���;同時(shí)����,眾多在美國已經(jīng)獲批上市的藥物�����,國內(nèi)尚無申報(bào)記錄,其中也不乏專利過期品種�����。無論是過度重復(fù)����,還是一家獨(dú)大,造成這種申報(bào)兩極分化的主要原因之一就是信息不對(duì)稱��。眾所周知����,藥品申報(bào)同樣存在黑箱期,在藥品申報(bào)公示或BE登記之前��,國內(nèi)企業(yè)的藥品立項(xiàng)品種和研發(fā)進(jìn)度����,外界無從獲悉。一旦企業(yè)完成相關(guān)申報(bào)研究之后�,即使出現(xiàn)多家申報(bào)的現(xiàn)象,恐怕更多的企業(yè)也不愿放棄,尤其耗費(fèi)了一定的研發(fā)費(fèi)用之后����。因此,就又出現(xiàn)新的重復(fù)申報(bào)品種���。總之�����,仿制藥的開發(fā)要綜合市場(chǎng)預(yù)期�����、企業(yè)戰(zhàn)略規(guī)劃��、生產(chǎn)線�����、業(yè)務(wù)優(yōu)勢(shì)�、外部競(jìng)爭(zhēng)環(huán)境等因素綜合考慮�。在當(dāng)下的仿制藥市場(chǎng)競(jìng)爭(zhēng)環(huán)境下�����,特別是國家集中采購已經(jīng)常態(tài)化之后,市場(chǎng)競(jìng)爭(zhēng)形勢(shì)已經(jīng)發(fā)生深刻改變���。越早獲悉競(jìng)品動(dòng)向��,越有可能避免扎堆����、減少研發(fā)浪費(fèi)��,更有助于將資源投入到回報(bào)率更高的研發(fā)活動(dòng)中���。