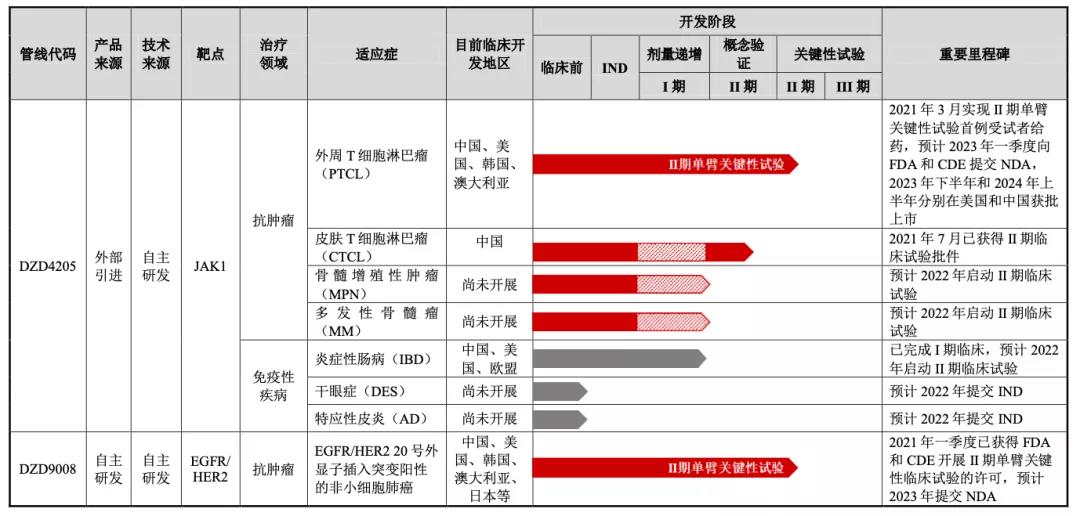
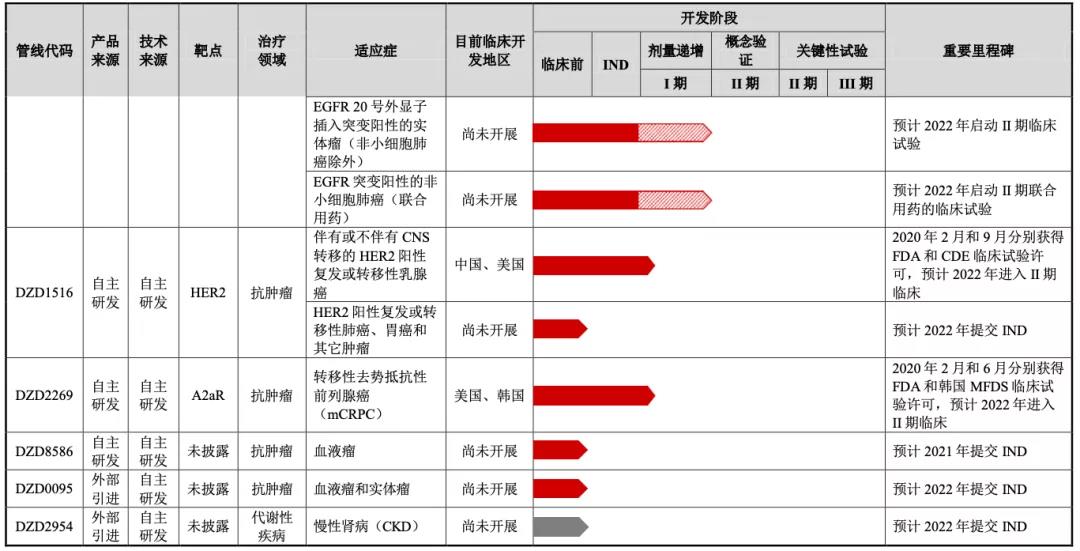
12月10日�����,迪哲醫(yī)藥正式在科創(chuàng)板鳴鑼上市���,發(fā)行價(jià)52.58元/股�����,合計(jì)募資約21億元��。冬日里的這抹亮色���,給國內(nèi)創(chuàng)新藥企在資本市場闖關(guān)的曲折一年��,畫下了柳暗花明的句點(diǎn)����。在它背后��,國投創(chuàng)新�����、紅杉資本����、禮來亞洲等早期投資者也因?yàn)樵?jīng)的信任和堅(jiān)持收獲了亮眼的成績單�����。2016年前后,跨國藥企陸續(xù)關(guān)閉了在中國開設(shè)的研發(fā)中心��。與同行們紛紛解散團(tuán)隊(duì)�����、關(guān)門歇業(yè)不同����,阿斯利康撤走了業(yè)務(wù)線,但留下了核心團(tuán)隊(duì)�。迪哲醫(yī)藥正是在原阿斯利康全球四大研發(fā)中心之一ICC基礎(chǔ)上,由國投創(chuàng)新及國投招商(先進(jìn)制造產(chǎn)業(yè)基金管理人)和阿斯利康聯(lián)合發(fā)起創(chuàng)立����,研發(fā)團(tuán)隊(duì)整建制來自原阿斯利康ICC。迪哲醫(yī)藥CEO張小林博士曾向媒體表示����,公司核心團(tuán)隊(duì)70%~80%的人員都是以前阿斯利康ICC的老同事,大家已經(jīng)磨合出了默契����,對新藥研發(fā)的流程也比較熟悉�����,在一致的目標(biāo)指引下����,藥物管線推進(jìn)流暢�,進(jìn)展也很喜人。IPO前�,迪哲醫(yī)藥的核心產(chǎn)品DZD4205和DZD9008已經(jīng)在中美兩地推進(jìn)到關(guān)鍵性試驗(yàn),前者是全球首個(gè)針對外周 T 細(xì)胞淋巴瘤疾病開展臨床研究的特異性JAK1抑制劑���,后者則是一種針對 EGFR/HER2 20 號外顯子插入突變設(shè)計(jì)的全球首創(chuàng) (First-in-class)小分子化合物���。此外,迪哲醫(yī)藥形成了腫瘤中樞神經(jīng)系統(tǒng)轉(zhuǎn)移研究平臺���、腫瘤免疫與放療聯(lián)合治療研究平臺���、生物標(biāo)志物的發(fā)現(xiàn)驗(yàn)證和臨床應(yīng)用技術(shù)、模型引導(dǎo)的藥物早期臨床研究技術(shù)(Model-Informed Drug Development����,MIDD)等與轉(zhuǎn)化科學(xué)相關(guān)的技術(shù)平臺�����,布局了豐富的小分子產(chǎn)品管線組合,是國內(nèi)少有的真正面向全球市場的創(chuàng)新藥企業(yè)�。國投創(chuàng)新及國投招商董事長高國華表示,“投資最終就是投資‘人’����,投資有企業(yè)家精神的優(yōu)秀科學(xué)家,是我們長期秉承的理念�。兼具專業(yè)性和情懷格局的張小林博士就是一位成功轉(zhuǎn)型企業(yè)家的優(yōu)秀科學(xué)家。迪哲醫(yī)藥堅(jiān)持源頭創(chuàng)新�,專注于惡性腫瘤及自身免疫性疾病等存在未被滿足和剛性治療需求的疾病領(lǐng)域,以推出全球首創(chuàng)藥(First-in-class)和具有突破性潛力的治療方法為目標(biāo)�����,所有產(chǎn)品均享有完整的全球權(quán)益��,并采用全球同步開發(fā)的模式���?����!?/span>2016年的冬天�,在MNC關(guān)閉中國研發(fā)中心的大潮中,阿斯利康總部也在計(jì)劃ICC的轉(zhuǎn)型��。ICC負(fù)責(zé)人張小林博士是資深的分子遺傳學(xué)專家����。上世紀(jì)末,張小林結(jié)束在哈佛大學(xué)醫(yī)學(xué)院癌癥中心的分子遺傳學(xué)博士后研究�,曾到美國波士頓大學(xué)生物分子基因工程中心工作2年,隨后加入阿斯利康��。回國組建ICC前���,張小林歷任阿斯利康的資深科學(xué)家�����、全球研發(fā)副總裁���,參與了阿斯利康一系列重磅新藥的早期開發(fā)。在ICC的10年��,張小林和團(tuán)隊(duì)有過不少高光時(shí)刻,除了主導(dǎo)并承擔(dān)阿斯利康肺癌新藥泰瑞沙在中國的研發(fā)任務(wù)�����,還把多個(gè)管線產(chǎn)品推進(jìn)到臨床試驗(yàn)�����。彼時(shí)����,與跨國藥企撤離相映成趣的��,是隨著國內(nèi)藥監(jiān)體系改革�����,和大量制藥人才從跨國藥企回流���,中國的創(chuàng)新藥生態(tài)正進(jìn)入成長的快車道��。在張小林內(nèi)心�,有意放手一搏���。他的想法很簡單�,要做國際領(lǐng)先的中國創(chuàng)新藥?����!拔覉?jiān)信當(dāng)下是本土生物醫(yī)藥產(chǎn)業(yè)謀求發(fā)展的好時(shí)機(jī)�����,無論是專業(yè)人員�����、政策�、資金、大環(huán)境各方面條件都非常利好���?���!焙髞?����,在向媒體回憶創(chuàng)業(yè)初衷時(shí),張小林仍然顯得堅(jiān)定��,“未來�����,我們將看到有一些本土創(chuàng)新藥企可以逐步走向世界�����,同樣希望看到更多出自本土研發(fā)的新藥真正打入國際市場�����?!?/span>那段時(shí)間���,張小林和國投創(chuàng)新生命科學(xué)團(tuán)隊(duì)負(fù)責(zé)人呂大忠的接觸變得頻繁���。呂大忠已經(jīng)帶領(lǐng)投資團(tuán)隊(duì)在生物醫(yī)藥領(lǐng)域深耕多時(shí),完成一系列初創(chuàng)企業(yè)布局后��,他們嘗試與跨國藥企探索合作的可能性��。因?yàn)橥顿Y團(tuán)隊(duì)很清楚,跨國藥企的研發(fā)����、醫(yī)學(xué)資源積累深厚,而初創(chuàng)企業(yè)專項(xiàng)突破能力強(qiáng)���、運(yùn)作靈活����,對于新藥創(chuàng)制而言�����,這些都是關(guān)鍵要素�����。所以當(dāng)阿斯利康有意對ICC進(jìn)行戰(zhàn)略調(diào)整時(shí)���,呂大忠及生命科學(xué)團(tuán)隊(duì)向阿斯利康提出建議�,希望張小林帶領(lǐng)整個(gè)ICC團(tuán)隊(duì)一起干�,“保留完整的有多年合作基礎(chǔ)的團(tuán)隊(duì),更有利于新公司研發(fā)進(jìn)度�����,去研發(fā)具有全球創(chuàng)新性的藥物?���!?/span>1+1>2的設(shè)想雖好,但畢竟沒有先例可循����,對于怎么推進(jìn),沒有太多頭緒���。反復(fù)商量過后�����,國投創(chuàng)新生命科學(xué)團(tuán)隊(duì)向阿斯利康拋出了全新合作方案。他們提出���,阿斯利康提供行業(yè)方面的全球視野和初始研發(fā)管線����,先進(jìn)制造提供資金和國內(nèi)資源支持����,支持管理團(tuán)隊(duì)持股����,阿斯利康�、先進(jìn)制造基金股權(quán)均等和張小林團(tuán)隊(duì)作為三方創(chuàng)始股東,于是有了迪哲醫(yī)藥��。新公司戰(zhàn)略性專注于惡性腫瘤等重大疾病以及免疫性疾病等存在未被滿足和剛性治療需求的疾病領(lǐng)域�����,把推出全球首創(chuàng)藥(First-in-class)和具有突破性潛力的治療方法作為目標(biāo)����。事實(shí)證明,創(chuàng)新投資模式下的迪哲醫(yī)藥成長速度很快���。第一年就著手申請兩個(gè)腫瘤靶向抑制劑的臨床批件���,同時(shí),迪哲醫(yī)藥陸續(xù)建立起了整合生物科學(xué)���、藥物化學(xué)�����、藥物ADME(機(jī)體對外源化學(xué)物的吸收��、分布���、代謝及排泄過程)等多個(gè)技術(shù)平臺��,覆蓋從藥物靶點(diǎn)發(fā)現(xiàn)與機(jī)理驗(yàn)證�����、轉(zhuǎn)化科學(xué)研究���、化合物分子設(shè)計(jì)與篩選、臨床前研究到CMC(藥品的化學(xué)�����、制造和控制)����、臨床方案設(shè)計(jì)與執(zhí)行的創(chuàng)新藥研發(fā)全流程���,在行業(yè)內(nèi)具有顯著的領(lǐng)先優(yōu)勢���。截至2021年6月30日����,一體化的研發(fā)平臺已經(jīng)幫助迪哲醫(yī)藥將包括DZD4025在內(nèi)的4個(gè)化合物從源頭自主發(fā)現(xiàn)并推進(jìn)到臨床階段����,形成了頗具創(chuàng)新性和差異化的小分子產(chǎn)品管線組合。幾乎是含著金湯匙出生的迪哲醫(yī)藥�����,一直都頗受外界關(guān)注����,這讓張小林壓力不小。與許多初創(chuàng)的新藥開發(fā)企業(yè)一樣�,迪哲醫(yī)藥把大量資金投入到研發(fā)中,收支很難平衡����。據(jù)招股說明書記載,2018年至2021年的前6個(gè)月,迪哲醫(yī)藥的研發(fā)費(fèi)用分別為21020.42萬元���、42143.56萬元�����、43949.48萬元和25773.68萬元����,累計(jì)超過13億元被用于產(chǎn)品管線的臨床前研究�、臨床試驗(yàn),加速產(chǎn)品研發(fā)進(jìn)程���。“以往在阿斯利康,更多考慮的是如何依據(jù)預(yù)算�����,在時(shí)間表中順利推動(dòng)項(xiàng)目的進(jìn)行�,完成既定目標(biāo)����。而迪哲則是一個(gè)獨(dú)立的公司����,我們根據(jù)我們手頭的資源�,力圖創(chuàng)造最大價(jià)值�。”張小林曾坦言�����,“角色的轉(zhuǎn)換���,做事思考方式和決策依據(jù)會有很大不同����。”迪哲醫(yī)藥的成長一直穩(wěn)定而高效���。兩款拳頭產(chǎn)品DZD4205和DZD9008都已經(jīng)處于中美雙報(bào)的關(guān)鍵性試驗(yàn)階段�����。其中�,迪哲醫(yī)藥計(jì)劃在2023年一季度分別向美國FDA(美國食品藥品監(jiān)督管理局)和中國NMPA(國家藥品監(jiān)督管理局)提交NDA(新藥上市申請)�,順利的話,2023年下半年和2024年上半年將分別獲得美國FDA和中國NMPA批準(zhǔn)�����,DZD9008的中美兩地上市申請也計(jì)劃在2023年提交。盡管JAK/STAT是頗受關(guān)注的信號通道���,但更多的研究主要集中在自身免疫性疾病及骨髓增殖性腫瘤(MPN)。具體而言,目前全球只有兩款JAK1抑制劑在腫瘤相關(guān)適應(yīng)癥中獲批上市��,分別是諾華的磷酸蘆可替尼(Ruxolitinib)和新基的Fedratinib����,其全球范圍內(nèi)的批準(zhǔn)適應(yīng)癥為骨髓增殖性腫瘤(MPN)中的骨髓纖維化和真性紅細(xì)胞增多癥���。其中�,磷酸蘆可替尼(Ruxolitinib)已經(jīng)在中國用于治療骨髓纖維化�。數(shù)據(jù)顯示,DZD4205作為全球首個(gè)進(jìn)入T細(xì)胞淋巴瘤適應(yīng)癥關(guān)鍵性臨床試驗(yàn)的高選擇性JAK1抑制劑�,對復(fù)發(fā)難治性外周T細(xì)胞淋巴瘤(PTCL)療效顯著���,II期推薦劑量的客觀緩解率達(dá)到51.9%����。DZD9008在面向EGFR 20號外顯子插入突變非小細(xì)胞肺癌患者的II期臨床試驗(yàn)中���,關(guān)鍵研究劑量下最佳客觀緩解率ORR達(dá)到48.4%�����,疾病控制率達(dá)到90.3%�。迪哲醫(yī)藥在研管線 (數(shù)據(jù)來源:招股說明書)
此外,迪哲醫(yī)藥目前公司正在開展DZD1516首次應(yīng)用于人體的針對轉(zhuǎn)移性HER2陽性乳腺癌的I期臨床試驗(yàn)���,DZD2269則正在進(jìn)行針對轉(zhuǎn)移性去勢抵抗前列腺癌(mCRPC)患者的I期臨床試驗(yàn)等一些列臨床研究��。據(jù)招股說明書信息����,DZD1516是迪哲醫(yī)藥自主研發(fā)的一種具有穿透血腦屏障能力的高選擇性HER2小分子酪氨酸激酶抑制劑,針對伴有或預(yù)防中樞神經(jīng)系統(tǒng)轉(zhuǎn)移的HER2陽性乳腺癌和其它HER2陽性實(shí)體瘤���,而DZD2269是高選擇性腺苷A2a受體拮抗劑,用于高濃度腺苷環(huán)境下的腫瘤免疫治療��,首個(gè)適應(yīng)癥針對轉(zhuǎn)移性去勢抵抗性前列腺癌(mCRPC)�����。過去的4年里,國投創(chuàng)新團(tuán)隊(duì)一直陪伴在側(cè)����。他們協(xié)助完善公司治理架構(gòu)��、優(yōu)化管理機(jī)制����,讓迪哲醫(yī)藥的經(jīng)營得以很快進(jìn)入正軌,專注于新藥研發(fā)和商業(yè)化����?��!皫缀跏菑某闪⒌牡谝惶扉_始��,研發(fā)團(tuán)隊(duì)就投入了高強(qiáng)度的工作中�����?��!闭麄€(gè)迪哲項(xiàng)目組的成員在回憶起迪哲醫(yī)藥成立之初的情景,還頗有些激動(dòng)�。2020年8月����,在國投創(chuàng)新的推動(dòng)下,迪哲醫(yī)藥引入禮來亞洲基金����、紅杉資本�����、三一創(chuàng)新等頭部機(jī)構(gòu)�����,累計(jì)募資約1億美元A輪��,為創(chuàng)新研發(fā)注入了重要力量���。成立4年來���,迪哲醫(yī)藥的發(fā)展基本實(shí)現(xiàn)了國投創(chuàng)新及國投招商董事長高國華所預(yù)想的:在國際化平臺基礎(chǔ)上,充分發(fā)揮科學(xué)家團(tuán)隊(duì)的力量����,結(jié)合中國市場的快速發(fā)展,提升新藥創(chuàng)制的競爭力��,走入世界新藥研發(fā)的前沿梯隊(duì)��。數(shù)據(jù)顯示��,全球創(chuàng)新藥市場規(guī)模遠(yuǎn)超仿制藥及生物類似藥市場規(guī)模���。2019年�����,創(chuàng)新藥市場規(guī)模占全球制藥市場總規(guī)模的66.26%�,達(dá)到8877億美元��,預(yù)計(jì)2021年這一市場規(guī)模將到9787億美元��。無論對于迪哲醫(yī)藥還是早期的投資者����、推動(dòng)者,這或許都是一個(gè)值得期許的未來���。按照張小林最初的設(shè)想,迪哲醫(yī)藥的全部研發(fā)管線都擁有全球權(quán)益�����,所有的臨床研究都以國際多中心的方式開展���。目前,公司相繼在中國���、美國、澳大利亞���、日本、韓國、歐洲等國家和地區(qū)開展或啟動(dòng)了臨床試驗(yàn)����,這與國內(nèi)創(chuàng)新藥企近年來越發(fā)凸顯的出海需求不謀而合。實(shí)際上,對于從跨國藥企整編過來的團(tuán)隊(duì)而言�,做全球化的原創(chuàng)新藥幾乎是一種默契。一方面����,迪哲醫(yī)藥采用了目前全球主流的新藥開發(fā)模式�,即不斷加深對基礎(chǔ)科學(xué)和臨床科學(xué)的理解����,有效地洞察臨床未滿足的治療需求,基于轉(zhuǎn)化科學(xué)(Translational Science)研究能力開發(fā)能夠解決臨床痛點(diǎn)的新藥���,在轉(zhuǎn)化科學(xué)領(lǐng)域建立了多項(xiàng)核心技術(shù)平臺��,有針對性地開發(fā)首創(chuàng)性(First-in-class)或具有突破性治療優(yōu)勢的創(chuàng)新藥�����,形成較高的技術(shù)壁壘����。比如�,創(chuàng)新性地建立腫瘤藥物與放療研究平臺,擅長于生物標(biāo)志物的發(fā)現(xiàn)并將其應(yīng)用于藥物發(fā)現(xiàn)和臨床開發(fā)�,并在行業(yè)內(nèi)較早使用模型引導(dǎo)的藥物早期臨床研究技術(shù)(MIDD)指導(dǎo)新藥開發(fā)����。再如��,突破了藥物穿越血腦屏障等行業(yè)技術(shù)難點(diǎn)��。而迪哲醫(yī)藥研發(fā)管線中的主要候選創(chuàng)新藥DZD4205����、DZD9008�、DZD1516、DZD2269等均是公司轉(zhuǎn)化科學(xué)研究的典型應(yīng)用成果����。另一方面�����,迪哲醫(yī)藥研發(fā)團(tuán)隊(duì)的跨國藥研經(jīng)驗(yàn)也讓全球新藥的創(chuàng)制過程更加流暢����。他們大多在跨國制藥公司從事超過20年的創(chuàng)新藥物研發(fā)或臨床研究���,過往的經(jīng)驗(yàn)積累下了與全球臨床專家、患者溝通臨床需求與方案設(shè)計(jì)的豐富經(jīng)驗(yàn)����,也十分熟悉FDA��、EMA 及 NMPA 等主要國家和地區(qū)監(jiān)管機(jī)構(gòu)的注冊需求細(xì)節(jié)�,這種全球化的思維方式,能夠保證公司創(chuàng)新藥物臨床研究的高效��、順利推進(jìn)����。在向科創(chuàng)板遞交上市申請前��,還有一個(gè)小插曲�。根據(jù)最初的計(jì)劃����,迪哲醫(yī)藥將到美國去做IPO�。因?yàn)閷τ谶@群科學(xué)家而言,用全球新的思路做藥�����,企業(yè)成長到一定階段登陸美股�����,似乎是順理成章的事����。但張小林博士堅(jiān)持認(rèn)為迪哲醫(yī)藥根植于中國����,要做從中國走向全球的世界級創(chuàng)新藥企,所以上市地也一定要留在中國���。正值國家成立科創(chuàng)板給予創(chuàng)新企業(yè)登陸資本市場的新機(jī)會,也是在國投創(chuàng)新和無錫市政府的推動(dòng)下���,迪哲醫(yī)藥成為科創(chuàng)板第8家采用第五套標(biāo)準(zhǔn)上市的醫(yī)藥企業(yè)��。對于剛剛過了4周年的迪哲醫(yī)藥來說,IPO是外界對它過去成績的一種認(rèn)可���,但更像一個(gè)成人禮。凡為過往���,皆是序章����,對于這家快速發(fā)展的創(chuàng)新藥企而言��,如何將全球新的藥物推向市場����,惠及更多患者,是市場對它的考驗(yàn)�,更是期待。
文章來源:動(dòng)脈網(wǎng)